
1. Die Ausgangssituation des Osmose-Prozesses
2. Der Osmose-Prozess
3. Abgeschlossener Osmose-Prozess
Der Umkehrosmose-Prozess
1. Die Ausgangssituation des Umkehrosmose-Prozesses
2. Der Umkehrosmose-Prozess
3. Abgeschlossener Umkehrosmose-Prozess
Zusammenfassung und Bedeutung der Begriffe aus diesem Artikel
Wie funktioniert die Umkehrosmose?
Die Umkehrosmose basiert auf dem umgekehrten Prinzip der aus der Natur bekannten Osmose.
Bei einem Osmose-Vorgang wird z. B. Wasser, welches frei von gelösten Stoffen (Salzen) ist, durch eine feine Barriere (semipermeable = halbdurchlässige Membran) auf die andere Seite strömen (diffundieren), wo sich mehr gelöste Teilchen befinden. Die Konzentration der Teilchen bezieht sich darauf, wie viel von einem Stoff in der Lösung vorhanden (gelöst) ist. Als Beispiel kann man gelöstes Speisesalz im Wasser nennen. So funktioniert Osmose als natürlicher Prozess, bei dem Konzentrationsunterschiede ausgeglichen werden.
Das Prinzip der Osmose einfach erklärt
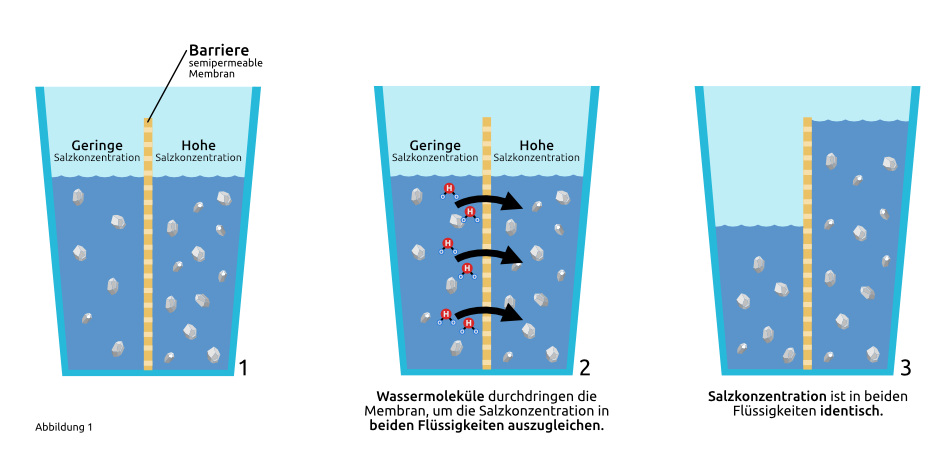
Die Abbildung zeigt in drei Schritten den Prozess der Osmose.
1. Die Ausgangssituation des Osmose-Prozesses
Stellen Sie sich ein Glas vor, welches in der Mitte durch eine Barriere aus z. B. Papier (Zellulose) getrennt ist.
Auf der linken Seite haben wir Wasser, in dem sehr wenig Speisesalz gelöst ist. Das Wasser schmeckt, wenn sie es kosten würden, nicht salzig. Auf der rechten Seite haben wir die gleiche Wassermenge, jedoch mit z. B. einem Teelöffel Salz gelöst. Wenn Sie jetzt das Wasser trinken würden, würde es salzig schmecken.
2. Der Osmose-Prozess
Beim Osmose-Prozess wollen die beiden Flüssigkeiten, die durch die semipermeable Membran getrennt sind, die Konzentration der Salze ausgleichen. Und deshalb wandern die Wassermoleküle von der weniger salzhaltigen Lösung, welche sich auf der linken Seite befindet, durch die Barriere auf die rechte Seite hinüber, um einen Ausgleich der beiden Salzkonzentrationen zu erzielen. Verantwortlich dafür ist der osmotische Druck.
3. Abgeschlossener Osmose-Prozess
Ist der Prozess der Osmose abgeschlossen, sind beide Lösungen von der Anzahl der gelösten Salze identisch. Würden Sie jetzt das linke und rechte Wasser kosten, würden beide Wässer gleich salzig schmecken.
Der Umkehrosmose-Prozess
Damit die natürliche Osmose umgekehrt werden kann, muss man zusätzlich Energie in Form von Druck aufwenden.
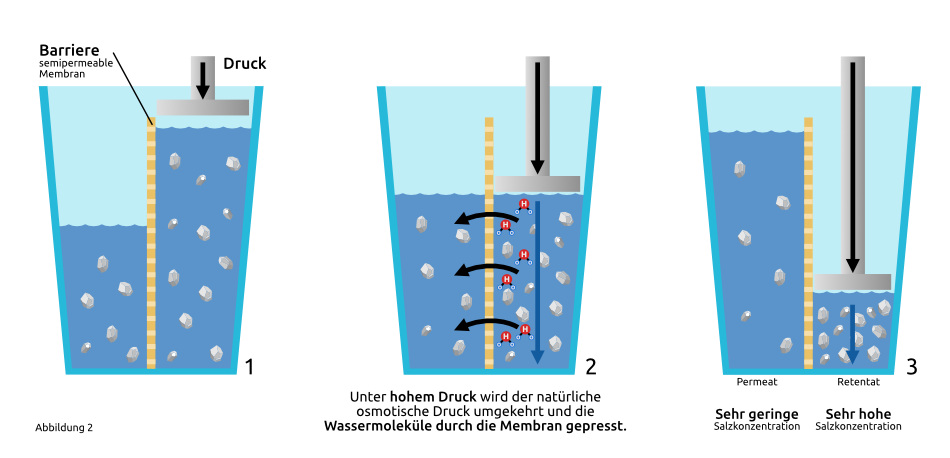
Die Abbildung zeigt in drei Abschnitten den Umkehrosmose-Prozess. Hier kommen die ersten Umkehrosmose-Fachbegriffe mit ins Spiel.
1. Die Ausgangssituation des Umkehrosmose-Prozesses
Stellen Sie sich jetzt einen Kolben in unserem Glas vor, der das Wasser auf der rechten Seite langsam nach unten drückt. Dieser Druck hilft, die Osmose umzukehren, indem er dem osmotischen Druck entgegenwirkt. Wir haben bereits erklärt, was der osmotische Druck ist.
2. Der Umkehrosmose-Prozess
Drückt der Kolben mit hohem Druck auf die rechte Seite im Glas, wird der osmotische Druck überwunden und nur die Wassermoleküle wandern durch die Barriere (semipermeable Membran) wieder zurück auf die linke Seite im Glas. Dieses Wasser, welches jetzt herüberwandert, wird Permeat genannt. Die Salzkonzentration auf der rechten Seite steigt an – dieses Wasser wird Retentat genannt. Auf der linken Seite fällt logischerweise die Salzkonzentration, da das dort vorhandene Salz in einer größeren Wassermenge gelöst wird.
3. Abgeschlossener Umkehrosmose-Prozess
Ist der Umkehrosmose-Prozess abgeschlossen, würde das Wasser auf der rechten Seite aufgrund der erhöhten Konzentration extrem salzig schmecken. Auf der linken Seite ist der Salzgehalt stark verdünnt, Sie würden es kaum noch schmecken.
Zusammenfassung und Bedeutung der Begriffe aus diesem Artikel
Osmotischer Druck:
Entsteht zwischen zwei Flüssigkeiten, die durch eine semipermeable Membran voneinander getrennt sind. Dabei bewegt sich ein Lösungsmittel (Wasser) von einer Seite mit niedrigerer Molekülkonzentration (wenig Salz) zur Seite mit höherer Molekülkonzentration (viel Salz) bis beide Salzkonzentrationen identisch sind.
Semipermeable Membran:
Semipermeabilität beschreibt die Fähigkeit von Grenzflächen (Membranen) nur bestimmte Stoffe durchzulassen, während sie andere blockieren. Eine semipermeable Membran lässt beispielsweise das Lösungsmittel (Wasser) passieren, aber nicht die gelösten Stoffe (Salze).
Permeat:
Im Bereich der Umkehrosmose bezeichnet man als Permeat jenes Wasser, das die semipermeable Membran durch den Umkehrprozess passiert hat.
Retentat:
Im Bereich der Umkehrosmose bezeichnet man als Permeat jenes Wasser, das die semipermeable Membran nicht passiert hat und eine hohe Konzentration an Salzen beinhaltet. Oft spricht man hier auch von Abwasser.
VISION AQUA® Umkehrosmoseanlagen und Wasserfilter

Average rating of 5 out of 5 stars
Scope of delivery:1 x VA Basic PLUS1 x VA-Standard - 500 GPD Membrane - Filmtec Material1 x VA-Standard - Sediment-Filter, PP cartridge (pre-filter)1 x VA Standard - Granulated Activated Carbon Filter, GAC Cartridge (post-filter)1 x Booster Pump 800 GPD - DirectDrive Brushles 24V - 2 x 3/8" tube outer diameter1 x Pressure switch - 1-10 Bar - 1/4" external thread - stainless-steel (incl. clamp for assembly)1 x installation set1 x 1-way tap, tap with straight connector - 1/4" tube external diameter (set)Hints!The system is delivered dry and has not been flushed!The system must first have produced 10-15 liters of water before it can be used for drinking water production.

Average rating of 5 out of 5 stars
Scope of delivery:1 x VA Basic PLUS1 x VA-Standard - 500 GPD Membrane - Filmtec Material1 x VA-Standard - Sediment-Filter, PP cartridge (pre-filter)1 x VA Standard - Granulated Activated Carbon Filter, GAC Cartridge (post-filter)1 x Booster Pump 800 GPD - DirectDrive Brushles 24V - 2 x 3/8" tube outer diameter1 x Pressure switch - 1-10 Bar - 1/4" external thread - stainless-steel (incl. clamp for assembly)1 x DC converter SD-100A-24 - 24V / 4.2A - Mean Well1 x installation set1 x 1-way tap, tap with straight connector - 1/4" tube external diameter (set)Hints!The system is delivered dry and has not been flushed!The system must first have produced 10-15 liters of water before it can be used for drinking water production.

Scope of delivery:1 x VA Basic1 x VA-Standard - 100 GPD Membrane - Filmtec Material1 x VA-Standard - Sediment-Filter, PP cartridge1 x VA Standard - Granulated Activated Carbon Filter, GAC Cartridge1 x Plastic tube for inlet - 1/4", 6.35 mm - color: yellow - John Guest, length: 2 m1 x Plastic tube for waste water - 1/4", 6.35 mm - color: red - John Guest, length: 2 m1 x Tap connector adapter with aerator and return for wastewater - M22 inner thread to 1/41 x M24 AG to M22 AG long version - water filter faucet adapter1 x M24 AG to M22 AG - water filter faucet adapter1 x 1/4" tap with stainless steel folding spout3 x filter cap - suitable for VA standard filter cartridgeHints!The system is delivered dry and has not been flushed!The system must first have produced 10-15 liters of water before it can be used for drinking water production.
Weitere Blogbeiträge zum Thema Trinkwasser

Sauberes Wasser für digitale Felder
Wasser wissen

Abkochverfügung für 20.000 Menschen im Landkreis Rosenheim
Wasserabkochmeldungen

Gefährliche Bakterien im Leitungswasser der Uniklinik Essen nachgewiesen
Wasserabkochmeldungen
Bleiben Sie auf dem Laufenden!

